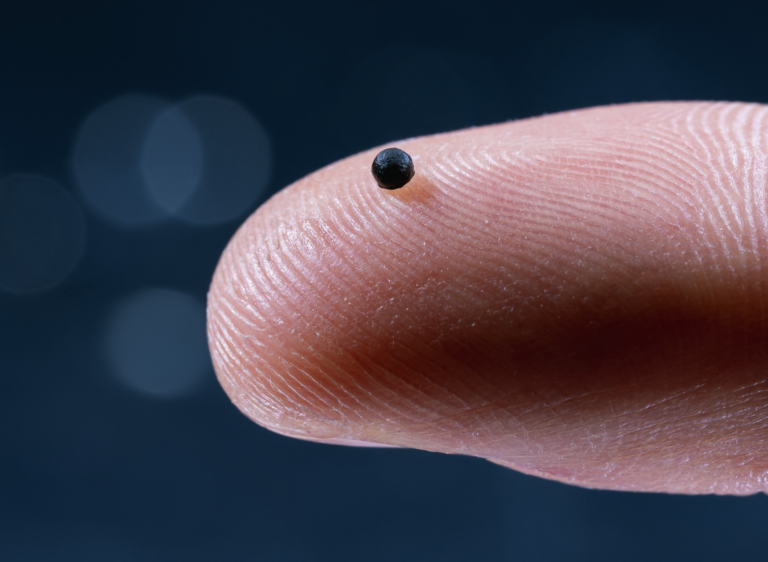
Garantire che il farmaco venga rilasciato esattamente dove occorre, senza farlo assumere in modo sistemico, scongiurando il rischio di effetti collaterali anche importanti (come le emorragie, sia lievi sia gravi, per i farmaci anticoagulanti). È l’obiettivo su cui lavora un gruppo di ricerca dell’ETH Zurich, il Politecnico federale di Zurigo, che sta perfezionando un microrobot – grande come un grano di pepe rosa – che può “navigare” ovunque nel corpo umano, con grande accuratezza e in modo indolore.
Descritti sulla rivista Science – così come su Science Robotics è visibile lo studio condotto dal California Institute of Technology (Caltech), negli Stati Uniti, focalizzato sullo sviluppo di microstrutture sferiche realizzate in “polietilenglicole diacrilato” (polimero versatile utilizzato soprattutto negli ambiti della scienza dei materiali e della biomedicina), che ha rivelato enormi potenzialità nel trasporto mirato di medicinali – i microrobot solubili e a guida magnetica sono già stati testati in un ambiente realistico. I ricercatori svizzeri, infatti, hanno creato alcuni modelli in silicone che riproducono, con estrema precisione, vasi sanguigni impiegati nella formazione medica, poi distribuiti dalla spin-off dell’ETH “Swiss Vascular”.
Il passo successivo? Le sperimentazioni cliniche, auspicando nuove opportunità in merito al trattamento mirato di patologie come l’ictus, provocato da un’insufficienza vascolare cerebrale improvvisa. Alcune sostanze, poi, potrebbero raggiungere meglio le cellule tumorali in aree poco accessibili del corpo. Parliamo di un microrobot assai diverso, per forma e dimensioni, dal modello “millepiedi” realizzato dai bioingegneri della City University di Hong Kong. Descritto su Science Robotics, questo minuscolo robot (“Fibot”) è in grado di trasportare medicinali in punti specifici dell’apparato digerente, senza lasciare tracce visibili del suo passaggio.
Come un videogioco
La sfida più importante che il team di ricerca, coordinato dai professori Salvador Pané Vidal e Bradley Nelson, ha dovuto affrontare riguardava le dimensioni: non è semplice, infatti, realizzare dispositivi così piccoli da passare all’interno dei capillari e che, in parallelo, siano perfettamente manovrabili, tracciabili e in grado di trasportare il farmaco desiderato. Per riuscirci, i ricercatori hanno fornito il minuscolo robot di due tipi di nanoparticelle: quelle di ossido di ferro trattate con zinco consentono di manovrare la capsula, che viene immessa attraverso un catetere speciale, inserito un grande vaso sanguigno (ad esempio, l’arteria femorale), per poi essere guidata da un operatore che utilizza una manopola simile ai joystick dei videogame, per il rilascio del principio attivo all’interno del corpo; le nanoparticelle di tantalio, invece, sono un metallo essenziale per l’osservazione della capsula ai raggi X mentre viaggia nei vasi sanguigni.
È bene sottolineare che, appena toccato il punto di rilascio, la capsula viene “parcheggiata” e, da qui, generato un campo magnetico che si inverte in modo costante e rapido, facendo vibrare (e scaldare) la capsula stessa. Il calore fa scomporre il guscio di gelatina che conserva il farmaco, raggiungendo la cellula da trattare. Quanto rimane della gelatina e del ferro viene espulso normalmente dall’organismo, mentre in tantalio prevede un lasso di tempo po’ più ampio.
Navigazione complessa
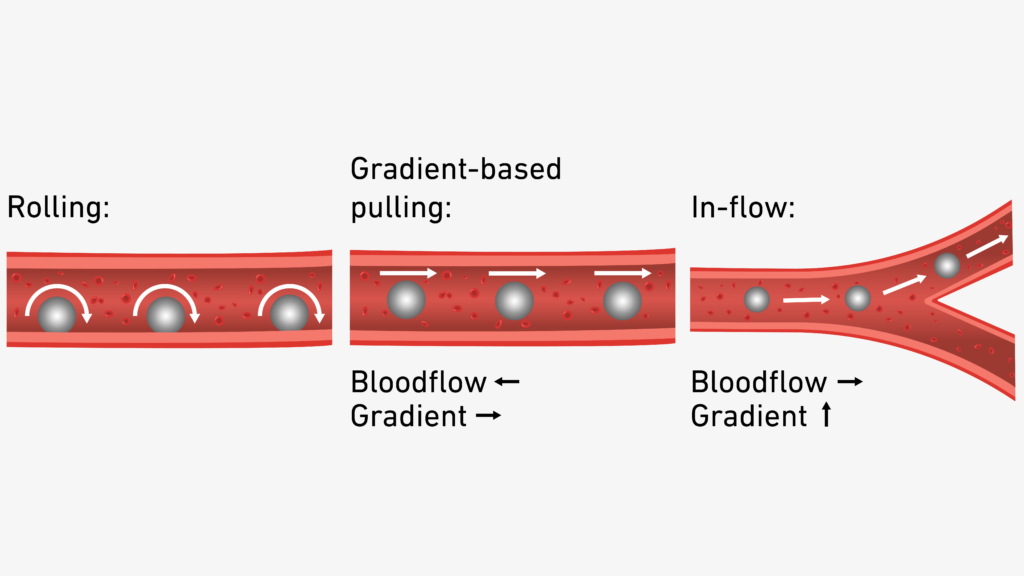
“Conciliare la funzionalità magnetica, la qualità dell’immagine e il controllo preciso in un unico microrobot ha previsto una perfetta sinergia tra la scienza dei materiali e l’ingegneria robotica, richiedendo molti anni per essere raggiunta con successo”, il commento del professor Nelson. Che, insieme al collega Pané Vidal e all’intero team si è dovuto rapportare a un’ulteriore criticità: condurre il minuscolo robot con estrema precisione, guidandolo nella direzione corretta davanti a una biforcazione dei vasi sanguigni oppure muovendolo controcorrente rispetto al flusso del sangue.
Anche in questo caso il team di ricerca dell’ETH Zurich ha trovato una soluzione, combinando tre differenti strategie di navigazione magnetica (“la velocità del flusso sanguigno nelle arterie varia a seconda della posizione. Ciò rende la navigazione di un microrobot assai complessa”, le parole di Nelson). Il risultato ottenuto è stato notevole, attraverso il rilascio del farmaco nel punto corretto in oltre il 95% dei casi.
L’universo dei microrobot, insomma, è contraddistinto da una moltitudine di tipologie e materiali, nonché di sistemi propulsivi e meccanismi di azione. Ragione per le loro possibili applicazioni sono vastissime e, in larga parte, ancora da scoprire.