Il neridronato per l’edema osseo si è rivelato molto efficace con buoni risultati per oltre l’80% dei pazienti.
L’edema osseo colpisce più frequentemente le donne tra i 50 e i 70 anni causando forti crisi dolorose. Le cause sono ancora in fase di studio.
Oggi può essere riconosciuto attraverso una RM, ma spesso può essere confuso con problematiche di tipo articolare.
Durante il meeting “Bone Edema & small implants“ saranno presentate le possibilità diagnostiche e le terapie farmacologiche e chirurgiche attualmente disponibili.

Esperti internazionali di Ortopedia e Reumatologia si confronteranno a Milano durante il meeting – masterclass SIGASCOT (Società Italiana di Chirurgia del Ginocchio, Artroscopia, Sport, Cartilagine e Tecnologie Ortopediche) “Bone Edema & small implants” in programma venerdì 3 e sabato 4 marzo 2017 al Sole 24 Ore e patrocinato dalle società scientifiche SIOT, ESSKA, SIOMMMS e SIR.
«Per anni abbiamo attribuito la responsabilità di dolori articolari, provenienti in particolare dal ginocchio e a manifestazione improvvisa quanto ingiustificata, a menischi, cartilagini o ad altre strutture articolari, senza capire quale fosse la loro vera causa – spiega Massimo Berruto, responsabile della Struttura Semplice Dipartimentale di Chirurgia Articolare del Ginocchio del Pini-CTO. – Grazie alla Risonanza Magnetica e attraverso una lettura sempre più attenta e approfondita delle immagini che questa strumentazione è in grado di produrre, l’attenzione del mondo radiologico, ortopedico e reumatologico si è concentrata sempre di più sul Bone Edema. In particolare vengono evidenziate dalla Risonanza quelle aree di osso limitrofe all’articolazione (ginocchio, anca, caviglia) che assumono un aspetto diverso, più sfumato, di colore grigio chiaro rispetto alla circostante area di osso che appare di colore più definito, un grigio scuro tendente al nero. Nella maggior parte dei casi quell’area grigio chiara corrisponde alla sede del dolore».
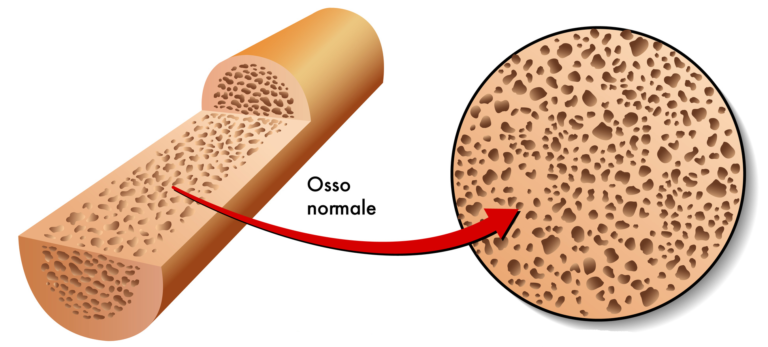
L’edema osseo
Quando un osso spugnoso, di solito riccamente innervato, improvvisamente non lo è più, è sottoposto a una sofferenza, si imbibisce, perde in contenuto di calcio, diventa più fragile e inizia a fare male. Va così incontro a una sorta di infarto, causa di intensi dolori che si manifestano soprattutto di notte e senza apparenti motivi o traumi evidenti.
Fitte e dolori sono i primi sintomi del Bone Edema, cioè l’edema dell’osso, una patologia a volte sottovalutata o confusa con altre problematiche di tipo articolare.
A livello di ginocchio gli edemi possono manifestarsi in seguito a traumi contusivi o distorsivi (vengono comunemente chiamati dagli anglosassoni “bone bruise” contusioni ossee) oppure sono dovuti a improvvisi cedimenti strutturali. Ma le cause sono ancora in fase di studio.
Pietro Randelli, direttore della 1° Clinica Universitaria di Ortopedia e Traumatologia e presidente SIGASCOT afferma: «La maggior parte degli edemi si verifica in pazienti sopra i 50 anni nei quali un iniziale stato artrosico può determinare un cedimento dei menischi, un danno a livello della cartilagine, una microfrattura ossea. Tutti questi eventi si traducono in un sovraccarico dell’osso spugnoso che si trova al di sotto della cartilagine, con un una sua temporanea sofferenza e il conseguente sviluppo di un edema più o meno diffuso».
A essere colpite dal problema sono soprattutto le donne di età compresa fra i 50 e i 70 anni, in sovrappeso, ma anche gli sportivi over 50 e i runner.
«In genere, da un giorno all’altro, il paziente riferisce la comparsa di un dolore articolare improvviso, non relazionato a traumi, molto intenso, senza apparenti cause scatenanti e particolarmente acuto nelle ore notturne – approfondisce Berruto. – La diagnosi viene sempre effettuata tramite Risonanza Magnetica, esame che se viene eseguito troppo precocemente potrebbe non evidenziare immediatamente l’edema. Gli edemi ossei possono infatti manifestarsi anche 6 settimane dopo la comparsa del dolore. Più raramente, viene effettuata la scintigrafia».
Il trattamento dell’edema osseo
Gli studi sull’edema osseo sono ancora in corso. Diverse novità sono emerse anche nel recente congresso di Tel Aviv organizzato dalla Società Internazionale di Ricerca sulla Cartilagine (ICRS).
«In particolare è emerso che è sempre più importante studiare questo aspetto patologico: capirne le cause, avere un quadro più chiaro sulla possibile evoluzione reversibile o non reversibile, avere una valutazione per ciascuna tipologia di edema sulle terapie più adeguate – commenta Berruto -. Per il trattamento del Bone Edema è necessario comportarsi come in presenza di una frattura».
Massimo Varenna, responsabile della S.S. Diagnosi e Cura Osteoporosi e malattie metaboliche del Day Hospital di Reumatologia del Pini-CTO è uno dei massimi esperti internazionali nel campo della terapia farmacologica dell’edema osseo. I suoi studi sono stati pubblicati sulla prestigiosa rivista “Reumatology“. Proprio Massimo Varenna ha messo a punto un trattamento con farmaci già utilizzati per l’osteoporosi: i neridronati. Questi, somministrati ad alti dosaggi per via endovenosa, si sono rivelati molto efficaci nel trattamento dell’edema osseo, con buoni risultati per oltre l’80% dei pazienti.
«In seguito alla diffusione e all’elevata incidenza di questa patologia spesso è necessario anche intervenire chirurgicamente: tra le tecniche introdotte di recente, in particolare per l’intervento all’anca e al ginocchio c’è la Core decompression che consiste nella perforazione dell’osso sofferente in modo da rivitalizzarlo, riducendone la pressione locale e stimolando la rivascolarizzazione e la subchondroplasty, cioè il riempimento e il rinforzo dell’osso sofferente con osso sintetico» – illustra Bruno Marelli, direttore del Dipartimento di Ortotraumatologia dell’ASST Pini-CTO.
Gli esiti del trattamento dell’edema osseo
L’evoluzione dell’edema osseo infatti può essere duplice. Se riconosciuto e trattato in tempo può regredire nel giro di qualche mese, non lasciando più tracce di sé. Questo si verifica in più dell’80% dei casi.
In caso di diagnosi sbagliata, ritardata o di edemi particolarmente diffusi o aggressivi, l’evoluzione del Bone Edema può essere negativa. In questi casi l’edema si riduce fino a scomparire, ma lascia un’area di necrosi (osteonecrosi).
«Si può ritornare al paragone con l’infarto: infatti l’osteonecrosi è una pastiglia di osso e cartilagine morta, non più vitale. In questi casi il dolore persiste e molto spesso è necessario ricorrere a un rivestimento dell’area di necrosi con una protesi» – conclude Massimo Berruto.