L’immunoterapia specifica sublinguale SLIT per l’asma allergico da acaro è stata inserita nelle linee guida Global Strategy for Asthma Management and Prevention 2017.

La Global Strategy for Asthma Management and Prevention, realizzato dalla Global Initiative for Asthma (GINA), rappresenta una delle più importanti risorse pratiche dedicate ai medici specialisti per la gestione del paziente asmatico e, dall’edizione 2017, include anche la raccomandazione dell’utilizzo dell’immunoterapia sublinguale (SLIT, Sublingual Allergen Immunotherapy).
L’indicazione, dedicata ai livelli di cura 3 e 4, precisa di considerare l’aggiunta dell’immunoterapia allergene-specifica sublinguale (SLIT) nei pazienti adulti sensibilizzati all’acaro della polvere, con rinite allergica, che manifestano esacerbazioni asmatiche nonostante l’assunzione di corticosteroidi inalatori (ICS), e in cui il Volume Espiratorio Massimo nel 1° secondo (FEV1) sia >70% del valore predetto.
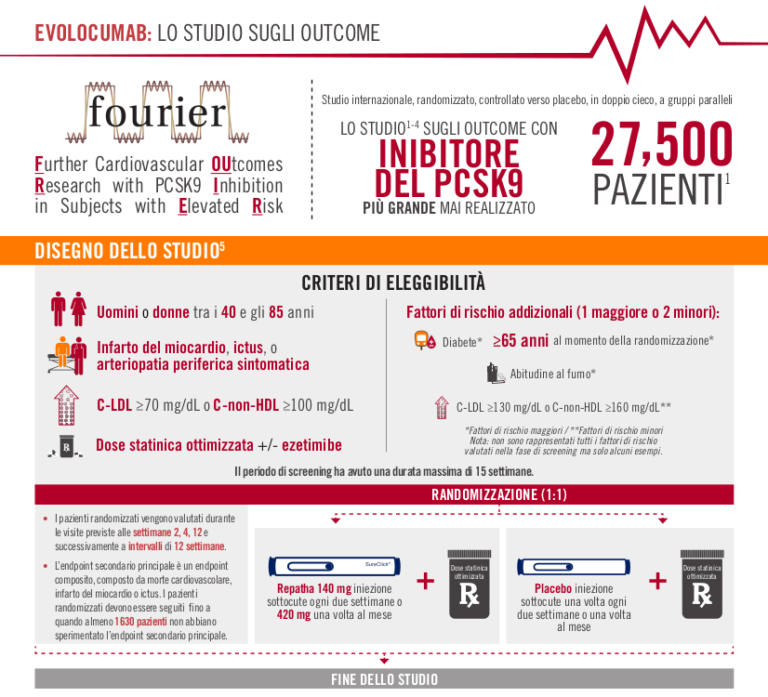
L’inserimento della SLIT nelle linee guida GINA è basato sulle evidenze emerse da uno studio pubblicato sulla rivista internazionale The Journal of the American Medical Association (JAMA) che ha dimostrato l’efficacia della SLIT-tablet nel trattamento dell’asma allergico da acaro della polvere. [Virchow JC, Backer V, Kuna P, et al. JAMA 2016;315(16):1715-25. doi: 10.1001/jama.2016.3964].
«Le linee guida GINA vanno oltre alla semplice raccomandazione di appropriatezza nella gestione della malattia asmatica e sono un documento costantemente aggiornato, basato sull’evidenza, per l’approccio alla gestione dell’asma nella pratica clinica – dichiara Pierluigi Paggiaro, delegato italiano per le Linee Guida GINA e membro del Comitato Scientifico del Progetto HOME – La SLIT (Immunoterapia Sublinguale) ha dimostrato di apportare benefici rilevanti nel trattamento dell’asma allergico non ben controllato e rappresenta una nuova arma a disposizione di medici e, soprattutto, pazienti, per poter gestire la patologia, quando altre soluzioni terapeutiche non determinano l’effetto desiderato».
Fino ad oggi, i pazienti affetti da allergia all’acaro della polvere, avevano a disposizione opzioni terapeutiche che consentivano di ottenere soltanto una riduzione dei sintomi, attraverso l’uso di corticosteroidi inalatori (ICS) e β2-agonisti a breve e lunga durata d’azione (rispettivamente SABA e LABA). I dati confermano, però, che, nonostante l’assunzione di tali trattamenti, fino al 30% dei pazienti continua a soffrirne. [Bateman ED, Boushey HA, Bousquet J, et al., GOAL Investigators Group. Can guideline-defined asthma control be achieved? the Gaining Optimal Asthma Control study, Am J Respir Crit Care Med. 2004;170(8):836-844].
«L’allergia da acaro della polvere è perenne – afferma Giorgio Walter Canonica, presidente della Società Italiana di Allergologia, Asma ed Immunologia Clinica (SIAAIC) e membro del Comitato Scientifico del Progetto HOME – Questo significa che chi ne è affetto è sempre esposto all’allergene e, quindi, se la malattia non è ben controllata, è anche sempre affetto dai sintomi che essa provoca. Avere un’ulteriore opzione terapeutica a disposizione, validata da un’istituzione autorevole come GINA, potrà avere un effetto positivo sulla qualità di vita del paziente».
«La SLIT ha dimostrato, oltre ai benefici terapeutici sul paziente affetto da asma allergico non ben controllato, anche vantaggi pratici nella gestione della terapia – afferma Francesco Blasi, presidente della Società Italiana di Pneumologia (SIP) e membro del Comitato Scientifico del Progetto HOME – Inoltre, è una terapia orale, che può essere assunta senza recarsi dal medico, con un conseguente risparmio in termini di tempo da parte sia del paziente, sia del medico, ed è gravata da meno effetti collaterali rispetto all’iniezione sottocute, soprattutto considerando gli shock anafilattici».
Altro aspetto da non sottovalutare, è la presenza concomitante di rinite allergica e asma bronchiale. Adriano Vaghi, responsabile del gruppo di studio BPCO, asma e malattie allergiche dell’Associazione Italiana Pneumologi Ospedalieri (AIPO) e membro del Comitato Scientifico del Progetto HOME spiega:
«Fino all’80% dei pazienti asmatici presenta anche rinite allergica, mentre circa il 30% dei pazienti con rinite allergica sviluppa nel tempo anche asma bronchiale. Le evidenze cliniche dimostrano che trattando correttamente le basse vie respiratorie per l’asma, si ottiene un miglioramento anche dei sintomi rinitici, e quindi un netto miglioramento della qualità della vita del paziente».
Il Progetto HOME
HOME (House-dust mite Observatory for the Management of the first Evidence-based immunotherapy) è un osservatorio, composto di un Board Scientifico che include alcuni tra i maggiori esperti di rinite e asma a livello nazionale, nato con l’obiettivo di indagare sui bisogni delle persone con allergia da acaro e di promuovere un’informazione scientificamente corretta e bilanciata.
Il progetto è patrocinato da 5 Società Scientifiche nazionali nell’ambito delle patologie respiratorie e allergiche:
- Società Italiana di Allergologia, Asma e Immunologia Clinica (SIAAIC),
- Società Italiana di Pneumologia (SIP),
- Associazione Allergologi Immunologi Territoriali Ospedalieri (AAITO),
- Accademia Italiana di Citologia Nasale – Accademia Italiana di Rinologia (AICNA – IAR),
- Associazione Italiana Pneumologi Ospedalieri (AIPO)
ed è realizzato con il sostegno non-condizionato di ALK Abellò.
Articoli correlati
Tiotropio Respimat per il controllo dell’asma in età pediatrica
Nuova indicazione di tiotropio Respimat per l’asma in Italia